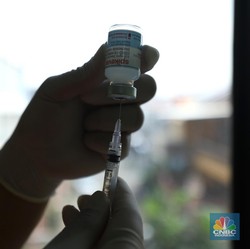
BPOM Kritik Tajam Uji Klinik Vaksin Nusantara Terawan, Gagal?

Jakarta, 博彩网站 - Badan Pengawas Obat dan Makanan (BPOM) telah melakukan penilaian terhadap hasil uji klinik fase I Vaksin Dendritik (AV-Covid-19) atau yang dikenal dengan Vaksin Nusantara.
Dalam surat yang diperoleh 博彩网站, dari hasil penelitian yang dilakukan oleh BPOM, data yang diperoleh dari interim fase I belum dapat mendukung rasionalitas untuk pelaksanaan uji klinik fase II dalam desain adaptive trial.
Sebab, diketahui dalam 4 minggu setelah penyuntikan, vaksin belum dapat memberikan respons yang memadai untuk melindungi subjek. Sehingga hal tersebut tidak memungkinkan digunakan dalam masa pandemi karena subjek tidak terlindungi.
Kepala BPOM Penny Lukito mengungkapkan, BPOM memberikan kesempatan kepada tim peneliti untuk memberikan klarifikasi terkait hal tersebut di atas dalam hearing Komite Nasional Penilai Obat dan tim ahli vaksin serta klinisi.
"Data tersebut sudah review sudah kami berikan surat dengan tembusan pada Kemenkes untuk mendapatkan respons dari tim peneliti. Untuk kemudian melakukan hearing dilakukan 16 Maret 2021," ujar Penny dalam Rapat Kerja dengan Komisi IX DPR RI, Rabu (10/3/2021).
Salah satu evaluasi yang menjadi sorotan BPOM terkait evaluasi aspek Cara Uji Klinik yang Baik. Berdasarkan data baseline imunogenitas yang diserahkan, semua subjek telah memiliki antibodi terhadap virus Covid-19 pada saat diikutsertakan pada uji klinik. Hal itu berbeda dengan protokol yang mengharuskan subjek yang direkrut adalah subjek yang belum terpapar virus Covid-19.
Kemudian, pada persetujuan uji klinik, masih terdapat ketidaksesuaian dengan protokol dan ketentuan pada Persetujuan Pelaksanaan Uji Klinik (PPUK). Kemudian persetujuan etik diberikan oleh Komite Etik RSPAD Gatot Subroto, bukan dari komite etik tempat uji klinik dilaksanakan yaitu di RS Kariadi Semarang.
"Kami sangat mendukung penelitian di dalam negeri. Namun tentunya Badan POM memastikan penelitian uji klinik pada manusia mengikuti good laboratory practice, good clinical trial practice, dan manufacturing practice. Tentunya Badan POM akan transparan. Kami tidak punya kepentingan menutupi apapun," ujar Penny.
"Namun ini suatu proses scientific perlu ini ditempatkan dalam forum scientific juga. Itulah kami menghormati etika penelitian sehingga kami ingin menyelesaikan dulu tahapan penelitian dengan peneliti. Pada 3 Maret surat kami yang ditujukan pada peneliti dari RSPAD, Puslitbangkes, RS Kariadi, sudah direspons dan kami juga beri kesempatan hearing," lanjutnya.
Lebih lanjut, Penny bilang proses itu harus diselesaikan terlebih dahulu dengan tim peneliti. "Sehingga memang saya dalam kesempatan ini juga tidak akan membahas data-data uji klinik tersebut karena forumnya belum tepat masih ada yang harus diproses dengan tim peneliti," katanya.
(miq/dru) Next Article Vaksin Terawan Terbukti Bisa Sembuhkan Penyakit? Ini Kata IDI


